När man vill kolla på en aminosyras laddningar via syra/basgrupper brukar man använda sig av pH 7,4 som referens, då det är detta pH som finns i de flesta levande organismer. Detta pH-värde kallas för fysiologiskt pH.
Aminosyror innehåller både en bas (aminogruppen) och en syra (karboxylgruppen). Vid fysiologiskt pH är aminogruppen positivt laddad, och karboxylgruppen negativt laddad. Detta sker eftersom:
- pKa för karboxylgruppen är lägre 7,4 (pKa ~ 2) , vilket innebär att den har lämnat ifrån sig sin proton.
- pKaH för aminogruppen är högre än 7,4 (pKaH ~ 9), vilket innebär att den har tagit upp en proton.
Notera att när vi i denna artikel beskriver pKa för en basisk grupp, så är det pKaH för den korresponderande syran som anges. pKaH = 9 för en aminogrupp syftar därmed på pKa för R-NH3+.
Aminosyror är zvitterjoner
När en molekyl innehåller både positiva och negativa laddningar, men totalt sett är oladdad kallas den för en zvitterjoner. Beroende på vilken aminosyra det handlar om, och vilket pH det är kan aminosyror vara zvitterjoner. Om vi kollar på den generella formen av aminosyror:

På grund av pKa-värdena kommer den generella aminosyran vid fysiologiskt pH (7,4) att ha tagit upp en proton med aminogruppen, och gett ifrån sig en proton via karboxylgruppen. Trots att det finns både positiva och negativa laddningar inom molekylen är oladdad. Den är i detta stadium en så kallad zvitterjon.
Om vi sänker pH i lösningen sker följande:
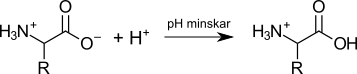
Aminosyrans karboxylgrupp tar upp en proton då det finns ett överskott av dessa i lösningen. Aminosyran är totalt sett positivt laddad.
Om vi istället höjer pH i lösningen:

Aminosyrans aminogrupp ger ifrån sig en proton då det finns ett underskott på protoner i lösningen. Aminosyran är totalt sett negativt laddad.
Isoelektrisk punkt för aminosyror
Alla aminosyror har olika sidokedjor. Beroende på vilken sidokedja det är, kommer den att påverka pKa-värdena för aminogruppen och karboxylgruppen en liten aning. Detta gör att det finns en variation i vilket pH-värde som aminosyran är neutral. Vissa aminosyror har egna sura eller basiska grupper i sina sidokedjor, och då kommer detta pH-värde att skilja sig mycket.
Det pH-värde där en molekyl är totalt sett oladdad och inte vandrar i ett elektriskt fält kallas för isoelektrisk punkt, och betecknas med pI (kallas ibland felaktigt för IP). Olika aminosyror har olika pI-värden. Exempel på detta kan ses i bilden nedan:

Eftersom pI varierar mellan de olika aminosyrorna är att det är möjligt att separera dem med olika typer av elektrofores. Läs mer om detta i våra artiklar om analytisk kemi.
Övningsuppgifter
Aminosyror är i sur lösning generellt sett negativt laddade. Rätt eller fel?
Fel. Aminosyror i sur lösning är generellt sett positivt laddade.
Aminosyror i en sur lösning upplever ett överskott av vätejoner (H+). Eftersom pH < pKa för de flesta syrabasgrupper i aminosyran kommer både aminogrupper och karboxylgrupper att vara protonerade. Detta innebär att aminogrupperna är positivt laddade, och karboxylgrupperna oladdade. Totalt sett finns det positiva laddningar i aminosyran.
Aminosyror i vattenlösning innehåller alltid laddningar. Rätt eller fel? Förklara varför.
Begreppet zvitterjon kan knuffa dig i rätt riktning vad gäller hur aminosyror beter sig i vattenlösning.
Rätt. I en vattenlösning går det i princip inte att ha en aminosyra utan laddningar i molekylen.
Vid ett neutralt pH beter sig aminosyran som en zvitterjon där karboxylgruppen (svag syra) har släppt ifrån sig en proton, och aminogruppen (svag bas) har tagit upp en proton, dvs det finns laddningar i molekylen. Om vi sänker pH (mer H+ i lösningen) kommer karboxylgruppen att ta upp en proton och bli oladdad, men aminogruppen är fortfarande positivt laddad. Om vi istället ökar pH (mindre H+ i lösningen) kommer aminogruppen att ge ifrån sig en proton och bli oladdad, men karboxylgruppen är fortfarande negativt laddad. Det går alltså inte att ha en aminosyra i vattenlösning utan interna laddningar.
Om man däremot kollar på molekylen som helhet kan den vara oladdad då de positiva och negativa laddningarna totalt sett kan ta ut varandra (exempelvis vid neutralt pH hos en aminosyra med sidokedja som varken är sur eller basisk).