Att identifiera ett okänt salt är en klassisk skolexempel när det kommer till kvalitativ analys. I den här artikeln går vi igenom hur detta fungerar samt berättar lite om bakgrunden till försöket.
Kort om ett salts uppbyggnad
 Låt oss säga att vi har ett okänt salt framför oss (som bilden till höger kan få symbolisera). Vårt uppdrag är nu att ta reda på vilket salt det är. Men hur gör man då detta?
Låt oss säga att vi har ett okänt salt framför oss (som bilden till höger kan få symbolisera). Vårt uppdrag är nu att ta reda på vilket salt det är. Men hur gör man då detta?
Ett sätt kan vara att titta på enkla saker som hur det ser ut eller luktar. Men i det här fallet säger det oss inte så speciellt mycket; precis som många andra salter är det till höger färg- och luktlöst.
Ett mer effektivt sätt är att titta på saltets positiva respektive negativa jonslag var för sig. Kommer vi till exempel fram till att den positiva jonen är Ca2+ och att den negativa är CO32−, räcker ju det för att konstatera att saltet i fråga måste vara kalciumkarbonat, CaCO3.
Lågfärgstest
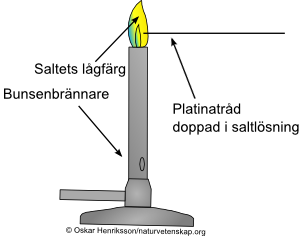 Ett enkelt sätt att ta reda på vilken positiv jon ett salt innehåller är genom att undersöka vilken lågfärg saltet i fråga ger. Ett sådant så kallat lågfärgstest genomförs genom att man för in en spatel med några saltkorn i lågan på en bunsenbrännare. Beroende på vilken positiv jon saltet innehåller förändras lågans färg på olika sätt. (Man kan också använda platinatråd doppad i en lösning av det okända saltet, som i bilden till höger.)
Ett enkelt sätt att ta reda på vilken positiv jon ett salt innehåller är genom att undersöka vilken lågfärg saltet i fråga ger. Ett sådant så kallat lågfärgstest genomförs genom att man för in en spatel med några saltkorn i lågan på en bunsenbrännare. Beroende på vilken positiv jon saltet innehåller förändras lågans färg på olika sätt. (Man kan också använda platinatråd doppad i en lösning av det okända saltet, som i bilden till höger.)
Orsaken till att lågan byter färg är att temperaturen blir så hög att elektronerna i saltjonernas yttersta elektronskal tar upp energi som de använder för att ”hoppa upp” till högre elektronskal än det de redan är i (man säger att jonerna exciteras). Detta tillstånd dock inte speciellt stabilt och det dröjer därför inte länge förrän elektronerna i fråga faller tillbaka till sina ordinarie elektronskal. Då avges (emitteras) samma mängd energi som togs upp vid excitationen i form av elektromagnetisk strålning.
Vilken våglängd den här strålningen får beror på vilken jon som sände ut den. För flera positiva joner (men däremot nästan inga negativa) får strålningen en sådan våglängd att vi uppfattar den som synligt ljus. Genomförs lågfärgstestet på ett salt med kopparjoner utsänds till exempel strålning om vi uppfattar som grönt ljus, medan ett strontiumsalt ger rött ljus. Nedan följer en lista med några joner som ger utmärkande lågfärger:
| Litium | Li+ | Röd-rosa | |
| Natrium | Na+ | Gul | |
| Kalium | K+ | Lila | |
| Barium | Ba2+ | Grön-orange | |
| Kalcium | Ca2+ | Orange | |
| Koppar | Cu2+ | Blå-grön | |
| Strontium | Sr2+ | Röd |
Kan du utifrån detta komma fram till vilket salt som fanns på platinatråden i bilden ovan, till höger?
Nej, det kan du inte. Det enda vi kan komma fram till är att saltets positiva jon sannolikt är Na+. Vilken den negativa jonen är återstår att ta reda på. Men hur gör man då det? Ett sätt är att göra ett fällningstest. Innan vi går närmare in på det behöver du dock en liten introduktion på svårlösliga salter och fällningar.
Kort om svårlöstliga salter och fällningar
Vi har tidigare sett att många salter är lättlösliga i vatten. Men faktum är att det finns en del undantag mot denna tumregel. Vissa salter vars joner har liknande storlek och/eller samma värde på sina laddningar hålls ihop av så pass starka jonbindningar att de tvärt om är i det närmaste olösliga i vatten. Några exempel på sådana salter är
– Kalciumkarbonat, CaCO3, vitt
– Bariumkarbonat, BaCO3, vitt
– Bariumsulfat, BaSO4, vitt
– Silverklorid, AgCl, vitt
– Silverjodid, AgI, gult
– Vissa hydroxider, såsom koppar(II)hydroxid, blått, järn(II)hydroxid, grönt, och järn(III)hydroxid, rödbrunt.
Det intressanta med detta är att om två saltlösningar blandas på ett sådant sätt att joner som kan bilda ett svårlösligt salt hamnar i samma lösning, kommer dessa att slå ihop sig och bilda detta svårlösliga salt. Låt oss titta på ett exempel på hur detta kan gå till.
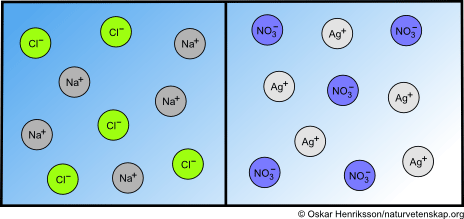
Tänk dig att vi har två saltlösningar: en natriumkloridlösning och en silvernitratlösning (symboliseras av modellen nedan). Eftersom båda dessa salter är lättlösliga i vatten kommer de att vara helt uppdelade i joner. Det intressanta händer när vi låter lösningarna blandas med varandra (klicka på bilden för att se vad, tryck backspace för att komma tillbaka).
Eftersom de upplösta jonerna kan röra sig hur som helst i vattnet kommer de ständigt att krocka med varandra. Då och då kommer alltså silver- och kloridjoner att mötas och när de väl gör det är blir det väldigt svårt för vattenmolekylerna att dela på dem eftersom silverklorid är i det nästan olösligt i vatten. Genast efter att natriumklorid- och silvernitratlösningarna har blandats börjar därför silver- och kloridjoner klumpa ihop sig till fasta bitar av silverklorid, vilket man kallar för att silverklorid fälls ut(se hur det ser ut i verkligheten på Youtube).
Reaktionsformeln kan skrivas på två sätt, antingen
\(\mathrm{Na^+(aq) + Cl^-(aq) + Ag^+(aq) + NO_3^-(aq) \longrightarrow}\\\longrightarrow\: \mathrm{AgCl(s) + Na^+(aq) + NO_3^-(aq)\,,\:eller}\\ \mathrm{NaCl(aq) + AgNO_3(aq) \longrightarrow\: AgCl(s) + NaNO_3(aq)}\,.\)
Den här typen av reaktioner, när ett svårlösligt salt fälls ut, kallas för fällningsreaktioner och regeln om att ett svårlösligt salt alltid fälls ut om joner som kan bilda det blandas är användbar till mycket. Bland annat när man ska rena avloppsvatten från fosfatjoner (som annars leder till övergödning i sjöar och vattendrag). Det är nämligen så att saltet aluminumfosfat är svårlösligt i vatten. Tillsätter man aluminiumjoner i reningsverket kommer dessa alltså reagera med fosfatjonerna och bilda en fällning av aluminiumfosfat, som man låter sjunka till botten i stora bassänger.
Fällningstest
Vattenrening är inte det enda man kan använda fällningsreaktioner till. De kan också hjälpa oss med att analysera ett okänt salt. Låt oss säga att vi har ett salt som vi misstänker innehåller kloridjoner. Genom att lösa upp det i vatten och tillsätta en lösning innehållande silverjoner kan vi enkelt konstatera om så är fallet eller inte. Bildas det en vit fällning tyder det på att saltet innehåller kloridjoner, medan saltet sannolikt inte innehåller kloridjoner som någon vit fällning inte bildas. Man säger att silverjoner kan användas för att påvisa kloridjoner, eller fungerar som reagens på kloridjoner.
Man kan förstås också göra tvärt om. Vill vi undersöka om ett salt innehåller silverjoner löser vi helt enkelt upp det i vatten och tillsätter en lösning med kloridjoner. Bildas en vit fällning tyder det på att saltet innehåller silverjoner. Kloridjoner kan alltså användas som reagens på silverjoner.
Ett annat exempel skulle kunna vara att vi vill undersöka om ett salt innehåller sulfatjoner. Då tillsätter vi en lösning med bariumjoner och ser efter om det bildas någon vit fällning. Men även om det gör det kan vi inte vara helt säkra, eftersom vi inte med blotta ögat kan se om fällningen som bildas är bariumsulfat, eller bariumkarbonat – båda är ju vita! Som tur väl är finns det ett sätt att skilja dessa båda fällningar åt, nämligen genom att tillsätta en syra.
Om den vita fällningen är bariumkarbonat kommer karbonatjonerna att reagera med syrans vätejoner och bilda vatten och koldioxid som syns som luftbubblor i lösningen, enligt formeln
\(\mathrm{BaCO_3(s) + 2H^+(aq) \longrightarrow\: Ba^{2+}(aq) + \underline{CO_2(g)} + H_2O(l)}\,.\)
Sulfatjoner kan däremot inte reagera på motsvarande sätt, vilket innebär att fällningen bör vara bariumsulfat om det inte bildas bubblor.
Övningsuppgifter
Dags för några frågor på det du nu har lärt dig! Vissa av frågorna är ganska svåra, men det viktigaste är inte att du klarar frågan utan att du efter att ha läst svaret förstår principen.
Ett salt ger orange lågfärg och ger i löst form en vit fällning vid tillsats av silvernitrat. Vilket salt bör det vara?
Den orange lågfärgen tyder på att den positiva jonen är Ca2+, medan fällningsreaktionen tyder på att den negativa jonen är Cl−. Saltet bör alltså vara kalciumklorid, som har formeln CaCl2.
Både strontiumnitrat och kaliumnitrat är vita salter i fast form. Beskriv hur du med ett enkelt experiment ändå kan skilja på dem.
Utför ett lågfärgstest. För in en spatel med lite av salterna (var för sig) i lågan på en bunsenbrännare. Det som då ger röd färg är strontiumnitrat, medan det som ger lila färg är kaliumnitrat.
I tre provrör har du vattenlösningar av tre olika salter; i provrör a har du litiumnitrat (LiNO3), i provrör b natriumjodid (NaI) och i provrör c kaliumklorid (KCl). I vart och ett av provrören tillsätts några droppar silvernitratlösning (AgNO3). I vilket/vilka av provrören får vi en vit fällning?
Vi tittar på provrören var för sig:
a) Här kommer inga joner som kan bilda ett svårlöslig salt komma i kontakt med varandra. Ingen fällning bildas alls.
b) Här hamnar silverjoner och jodidjoner tillsammans. Alltså kommer vi få en fällning av silverjodid, som dock inte är vit utan gul.
c) Här kommer silverjoner och kloridjoner att hamna i samma provrör, vilket innebär att de kommer att bilda den vita fällningen silverklorid.
Rätt svar är alltså provrör c.
Du har ett okänt salt framför dig. Nämn ett sätt att visa att saltet i fråga är järn(III)sulfat.
1. Lös lite av saltet i vatten och dela upp lösningen på två provrör.
2. Tillsätt sedan några droppar natriumhydroxidlösning till det ena. Bildas det då en rödbrun fällning innehåller saltet järn(III)-joner.
3. Tillsätt sedan bariumklorid till det andra röret. Bildas det en vit fällning innehåller saltet antingen karbonat- eller sulfatjoner.
4. Tillsätt saltsyra till det andra provröret. Om det inte bildas gasbubblor är karbonatjoner uteslutet och saltet måste vara järn(III)sulfat.
Den positva jonen i ammoniumklorid, NH4Cl, går inte att identifiera med ett lågfärgstest. Däremot kan den påvisas genom att man löser upp saltet i en kraftigt basisk lösning av (förslagsvis) natriumhydroxid och därefter kokar lösningen. Använd dina kunskaper om syror och baser för att förklara hur detta kan gå till!
Ammoniumjonerna kommer att avge en vätejon till den starka basen, varvid ammoniak bildas. När lösningen kokar kommer lösligheten för ammoniaken minska och ångor av ammoniak som lätt känns igen på doften avges. Man kan också påvisa ammoniaken genom att hålla ett fuktat pH-papper över provrörsmynningen; pH-pappret kommer då få en färg som motsvarar basisk reaktion. Det kan vara en god idé att använda dragskåp eftersom ammoniak är skadligt i stora mängder.
Fällningsreaktioner kan också användas för att utföra en enkel form av kvantitativ analys. Se om du klarar den här frågan!
Till en e-kolv med 200 cm3 lösning av saltet järn(II)klorid, FeCl2, tillsätts ett överskott av silvernitratlösning med koncentrationen 1,0 mol/dm3. Innehållet i provröret filtreras därefter och filterkakan tvättas och torkas noggrant. När detta är gjort väger den 5,27 g. Hur stor var koncentrationen av järn(II)klorid i ursprungslösningen?
Koncentrationen var 0,092 mol/dm3.
När silvernitratet tillsätts kommer silverjonerna och kloridjonerna från järn(II)kloriden att gå ihop och bilda silverklorid enligt formeln
\(\mathrm{FeCl_2 + 2AgNO_3 \longrightarrow\: 2AgCl(s) + Fe(NO_3)_2}\,.\)
Det innebär att det enda fasta ämne som finns i provröret innan filtreringen är silverklorid, som därmed måste vara det som filterkakan utgörs av.
Låt oss nu gå över till räknandet. Vi börjar med att räkna ut den substansmängd som de 5,27 grammen silverklorid motsvar:
\(n(\mathrm{AgCl})=\frac{{m}(\mathrm{AgCl})}{{M}(\mathrm{AgCl})}=\mathrm{\frac{5.27 g}{143.32 g/mol}=0.03677\,mol}\,.\)
Med hjälp av reaktionsformeln kan vi beräkna vilken mängd järn(II)klorid motsvarar. Enligt den gäller molförhållandet
\(\frac{{n}(\mathrm{FeCl_2})}{1}=\frac{{n}(\mathrm{AgCl})}{2}\,.\)
Alltså är
\(n(\mathrm{FeCl_2})=\frac{{n}(\mathrm{AgCl})}{2}=\mathrm{\frac{0.03677\,mol}{2}=0.018385\, mol}\,.\)
Vi vet med andra ord att det fanns 0,018385 mol järn(II)klorid i e-kolven från början. Volymen lösning var som bekant 200 cm3, eller 0,20 dm3 som det också kan skrivas, vilket innebär att
\(c(\mathrm{FeCl_2})=\frac{n(\mathrm{FeCl_2})}{{V}}=\mathrm{\frac{0.018385\,mol}{0.20\,dm^3}=0.091925\,mol/dm^3}\,.\)
Svar: Koncentrationen var (med två gällande siffror angiven) 0,092 mol/dm3.